Bạn đang xem: Bảng hóa trị kim loại

Bảng hóa trị của một số trong những nguyên tố hóa học thường gặp
Hóa trị của một nguyên tố hóa học được xác minh bằng tổng số link hóa học của nhân tố đó tạo cho trong phân tử. Cùng với hóa trị của một yếu tắc thì thầy đã và đang có một nội dung bài viết khác chia sẻ với các em nhiều hơn về hóa trị của một nguyên tố.Trong nội dung bài viết này, thầy chỉ share hóa trị của một số trong những nguyên tố thường xuyên gặp trong lịch trình hóa học lớp 8 giúp các em gồm thêm tứ liệu, tài liệu để củng cố kỹ năng hóa học cơ phiên bản của bản thân nhé. Những em có thể tham khảo thêmbảng hóa trị lớp 8 trang 42trong SGK nhé.Bảng hóa trị bao hàm có một số trong những thông tin như Số Proton, thương hiệu nguyên tố, cam kết hiệu hóa học, nguyên tử khối cùng cột cuối cùng hoàn toàn có thể hiện hóa trị của nguyên tố kia theo vần âm la mã. Bảng hóa trị bên dưới đây bao hàm tất cả gồm 30 nguyên tố hóa học thường mở ra trong lịch trình học hóa học lớp 8.Một số lưu ý với phần nhiều nguyên tố bao gồm nhiều hóa trị thường chạm chán như sắt kẽm kim loại có sắt, đồng . . . Còn phần nhiều nhiềunguyên tốphi kim sẽ có nhiều mức hóa trị không giống nhau như Nito, giữ huỳnh, phốt pho . . .
1. Bảng hóa trị của nhân tố hóa học thường xuyên gặp
| BẢNG 1- MỘT SỐ NGUYÊN TỐ HOÁ HỌC | ||||
| Số proton | Tên Nguyên tố | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
| 1 | Hiđro | H | 1 | I |
| 2 | Heli | He | 4 | |
| 3 | Liti | Li | 7 | I |
| 4 | Beri | Be | 9 | II |
| 5 | Bo | B | 11 | III |
| 6 | Cacbon | C | 12 | IV,II |
| 7 | Nitơ | N | 14 | II,III,IV… |
| 8 | Oxi | O | 16 | II |
| 9 | Flo | F | 19 | I |
| 10 | Neon | Ne | 20 | |
| 11 | Natri | Na | 23 | I |
| 12 | Magie | Mg | 24 | II |
| 13 | Nhôm | Al | 27 | III |
| 14 | Silic | Si | 28 | IV |
| 15 | Photpho | P | 31 | III,V |
| 16 | Lưu huỳnh | S | 32 | II,IV,VI |
| 17 | Clo | Cl | 35,5 | I,… |
| 18 | Argon | Ar | 39,9 | |
| 19 | Kali | K | 39 | I |
| 20 | Canxi | Ca | 40 | II |
| 24 | Crom | Cr | 52 | II,III |
| 25 | Mangan | Mn | 55 | II,IV,VII… |
| 26 | Sắt | Fe | 56 | II,III |
| 29 | Đồng | Cu | 64 | I,II |
| 30 | Kẽm | Zn | 65 | II |
| 35 | Brom | Br | 80 | I… |
| 47 | Bạc | Ag | 108 | I |
| 56 | Bari | Ba | 137 | II |
| 80 | Thuỷ ngân | Hg | 201 | I,II |
| 82 | Chì | Pb | 207 | II,IV |
2. Bảng hóa trị một số trong những nhóm nguyên tử
| Bảng II - một trong những nhóm - nơi bắt đầu axit | ||||
| STT | Tên nơi bắt đầu - nhóm chức | Công thức hóa học đội - cội axit | Nguyên tử khối | Hóa Trị |
| 1 | Hidroxit | OH | 17 | I |
| 2 | Clorua | Cl | 35,5 | I |
| 3 | Nitrat | NO3 | 62 | I |
| 4 | Sunfat | SO4 | 96 | II |
| 5 | Cacbonat | CO3 | 60 | II |
| 6 | Clorat | Cl O3 | 83.5 | I |
| 7 | Perclorat | Cl O4 | 99.5 | I |
| 8 | Đi Hidro Photphat | H2PO4 | 98 | I |
| 9 | Hidro Photphat | HPO4 | 97 | II |
| 10 | Photphat | PO4 | 96 | III |
Cl.
Tên nhóm | Hoá trị | Gốc axit | Axit tương ứng | Tính axit |
Hiđroxit(*) (OH); Nitrat (NO3) | I | NO3 | HNO3 | Mạnh |
Sunfat (SO4); Cacbonat (CO3) | II | SO4 | H2SO4 | Mạnh |
Photphat (PO4) | I, II, III | Cl | HCl | Mạnh |
(*): thương hiệu này dùng trong các hợp hóa học với kim loại. | PO4 | H3PO4 | Trung bình | |
CO3 | H2CO3 | Rất yếu hèn (không tồn tại) |
Axit phosphoric có công thức hóa học rất đầy đủ là H3PO4. Đây là 1 trong axit gồm tính lão hóa trung bình nhưng bọn chúng lại tẹo nên rắc rối cho học sinh bởi vì nó có thể tạo thành 2 loại muối cùng với 3 phương pháp khác nhau.a. Muối axit chứa gốc PO4H3PO4 có thể tạo muối bột axit vào hai bí quyết M(H2PO4)x cùng M2(HPO4)x với M là kim loại nào đó. Nhìn vào bí quyết trên họ sẽ thấy băn khoăn lắm yêu cầu không, vậy thì nên quan gần kề hợp chất rõ ràng dưới đây nhé.Lấy M là sắt kẽm kim loại Natri bao gồm hóa trị 1 họ được:- Na(H2PO4)- Na2(HPO4)Trên đó đó là 2 bí quyết muối axit.b. Muối trung hòa - nhân chính chứa gốc PO4Công thức muối trung hòa có đựng gốc PO4 gồm dạng: M3(PO4)x với:M là kim loạix là số hóa trị của kim loại M.
3. Biện pháp học thuộc hóa trị đơn giản nhất.
Hiện nay, trên mạng thôn hội có không ít bài ca hóa trị được thầy cô sáng tác với mục đích xuất sắc giúp học sinh đam mê rộng với môn hóa học. Mặc dù nhiên, với từng thầy cô sẽ sở hữu phong cách khác biệt nên đều bài ca hóa trị cũng không giống nhau.Trong đời học sinh, tôi đã có lần rất thành công xuất sắc với bài bác ca hóa trị sau đây. Các em tìm hiểu thêm để học tốt môn hóa nhé.Kali, Iot, HiđroNatri với Bạc, Clo một loài
Có hóa trị I bạn ơi
Nhớ ghi cho rõ kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cùng tương đương Bari
Cuối thuộc thêm chú Oxi
Hóa trị II ấy gồm gì cực nhọc khăn
Bác Nhôm hóa trị III lần
Ghi sâu trí tuệ khi cần phải có ngay
Cacbon, Silic này đây
Là hóa trị IV không ngày làm sao quên
Sắt kia nhắc cũng thân quen tên
II, III tăng và giảm thật phiền lắm thay
Nitơ rắc rối nhất đời
I, II, III, IV khi vậy nên VLưu huỳnh lắm lúc thi đấu khăm
Lúc II, thời gian VI khi nằm sản phẩm công nghệ IVPhotpho nói tới không dư
Nếu ai hỏi đến thì ừ rằng VBạn ơi cố gắng học chăm
Bài ca hóa trị trong cả năm vô cùng cần
Sau khi các em học thuộc lòng bài ca hóa trị bên trên thì hóa trị của rất nhiều nguyên tố có trong bảng hóa trị bên trên các em vẫn thuộc lòng. Mình không cần phải dùng bảng để tra cứu hay "" bài nữa nhé.
Để hoàn toàn có thể học giỏi môn Hóa thì việc ghi nhớ bảng hóa trị các nguyên tố hóa học là yêu ước bắt buộc. Đây cũng là kiến thức và kỹ năng cơ bạn dạng sẽ theo những em trong suốt quy trình học cung cấp 2, cung cấp 3 với giúp những em giải đúng mực các bài xích tập liên quan. Sau đây là những kiến thức về bảng yếu tắc hóa học lớp 8 thường gặp và bài bác ca hóa trị dễ học, dễ nhớ mà ttgdtxphuquoc.edu.vn Education muốn share đến các em.
Bảng hóa trị một vài nguyên tố hóa học thường gặp
Số proton | Tên Nguyên tố | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
1 | Hiđro | H | 1 | I |
2 | Heli | He | 4 | |
3 | Liti | Li | 7 | I |
4 | Beri | Be | 9 | II |
5 | Bo | B | 11 | III |
6 | Cacbon | C | 12 | IV, II |
7 | Nitơ | N | 14 | II, III, IV… |
8 | Oxi | O | 16 | II |
9 | Flo | F | 19 | I |
10 | Neon | Ne | 20 | |
11 | Natri | Na | 23 | I |
12 | Magie | Mg | 24 | II |
13 | Nhôm | Al | 27 | III |
14 | Silic | Si | 28 | IV |
15 | Photpho | P | 31 | III, V |
16 | Lưu huỳnh | S | 32 | II, IV, VI |
17 | Clo | Cl | 35,5 | I,… |
18 | Argon | Ar | 39,9 | |
19 | Kali | K | 39 | I |
20 | Canxi | Ca | 40 | II |
24 | Crom | Cr | 52 | II, III |
25 | Mangan | Mn | 55 | II, IV, VII… |
26 | Sắt | Fe | 56 | II, III |
29 | Đồng | Cu | 64 | I, II |
30 | Kẽm | Zn | 65 | II |
35 | Brom | Br | 80 | I… |
47 | Bạc | Ag | 108 | I |
56 | Bari | Ba | 137 | II |
80 | Thuỷ ngân | Hg | 201 | I, II |
82 | Chì | Pb | 207 | II, IV Chú thích: Chữ color đen: nguyên tố kim loạiChữ màu xanh: yếu tắc phi kim Chữ màu đỏ: nhân tố khí hiếm Hóa trị của thành phần là tổng số link hóa học mà lại nguyên tử của yếu tố đó làm cho trong phân tử. Bảng hóa trị sẽ bao hàm các thông tin quan trọng như thương hiệu nguyên tố, số proton, ký kết hiệu hóa học, nguyên tử khối cùng hóa trị của yếu tố đó. Trang bị tự của những nguyên tố vào bảng nguyên tố hóa học sẽ được bố trí theo số proton tăng dần. Tuy nhiên, những em buộc phải nhớ rằng, các nguyên tố hóa học chưa hẳn chỉ tất cả duy duy nhất một hóa trị. ở bên cạnh một số nguyên tố có một hóa trị như Hidro (I), Liti (I), Beri (II), Bo (III) thì gồm có nguyên tố có 2 hóa trị như Cacbon (II, IV), Photpho (III, V), Crom (II, III) hoặc nhiều hơn thế nữa 2 như Nitơ (II, III, IV), diêm sinh (II, IV, VI) tuyệt Mangan (II, IV, VII),… Bảng Tuần Hoàn những Nguyên Tố Hóa Học: bí quyết Học và Mẹo Ghi Nhớ Có bao nhiêu nguyên tố hóa học?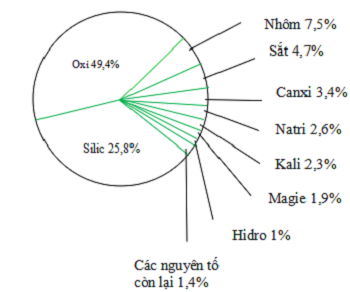 Hiện nay, các nhà khoa học đã tò mò được tổng số 110 yếu tắc hoá học. Trong đó, 98 nguyên tố hóa học có nguồn gốc từ tự nhiên và thoải mái (trên Trái Đất, phương diện trời, phương diện trăng…), những nguyên tố còn sót lại là nhân tạo. Bảng hóa trị một số trong những nhóm nguyên tử |









