Chương 2: Kim loại
• bài bác 15 : đặc thù vật lý của kim loại • bài xích 16 : tính chất hóa học của sắt kẽm kim loại • bài 17 : Dãy chuyển động hóa học của sắt kẽm kim loại • bài bác 18: Nhôm • bài bác 19: fe • bài xích 20: hợp kim sắt: Gang,thép • bài bác 21: Sự ăn uống mòn kim loại và bảo đảm an toàn kim loại không xẩy ra ăn mòn • bài bác 22: rèn luyện chương 2: kim loại • bài 23: thực hành : tính chất hóa học tập của nhôm cùng sắt • bài bác 24: Ôn tập học tập kỳ 1
Chương 3: Phi kim. Qua loa về bảng tuần hoàn các nguyên tố hóa học
• bài xích 25: đặc thù của phi kim • bài 26: Clo • bài 27: Cacbon • bài xích 28: các oxit của cacbon • bài 29: Axit cacbonic cùng muối cacbonat • bài 30: Silic. Công nghiệp silicat • bài 31: qua quýt về bảng tuần hoàn những nguyên tố hóa học • bài xích 32: rèn luyện chương 3: Phi kim - qua loa về bảng tuần hoàn các nguyên tố hóa học • bài xích 33: Thực hành: tính chất hóa học của phi kim và hợp hóa học của chúng
Chương 4: Hiđrocacbon. Nhiên liệu
• bài 34: tư tưởng về hợp hóa học hữu cơ và hóa học tập hữu cơ • bài xích 35: kết cấu phân tử hợp chất hữu cơ • bài xích 36: Metan • bài bác 37: Etilen • bài bác 38: Axetilen • bài 39: Benzen • bài 40: Dầu mỏ với khí vạn vật thiên nhiên • bài xích 41: nguyên nhiên liệu • bài 42: rèn luyện chương 4: Hiđrocacbon. Nguyên liệu • bài xích 43: Thực hành: đặc thù của Hiđrocacbon
Chương 5: Dẫn xuất của Hiđrocacbon. Polime
• bài xích 44: Rượu etylic • bài xích 45: Axit axetic • bài xích 46: Mối tương tác giữa etilen, rượu etylic với axit axetic • bài 47: Chất béo • bài 48: Luyện tập: Rượu etylic, axit axetic và chất mập • bài 49: Thực hành: đặc thù của rượu và axit • bài 50: Glucozơ • bài bác 51: Saccarozơ • bài xích 52: Tinh bột và xenlulozơ • bài 53: Protein • bài 54: Polime • bài xích 55: Thực hành: đặc điểm của gluxit • bài bác 56: Ôn tập cuối năm - Phần 1: Hóa vô sinh • bài bác 56: Ôn tập thời điểm cuối năm - Phần 2: Hóa cơ học
Mục lục Giải bài tập SGK chất hóa học 9 theo chương •Chương 1: các loại hợp chất vô cơ •Chương 2: kim loại •Chương 3: Phi kim. Sơ sài về bảng tuần hoàn các nguyên tố hóa học •Chương 4: Hiđrocacbon. Xăng •Chương 5: Dẫn xuất của Hiđrocacbon. Polime
- Chọn bài bác -Bài 15: đặc thù vật lí của kim loại
Bài 16: tính chất hóa học của kim loại
Bài 17: Dãy chuyển động hóa học tập của kim loại
Bài 18: Nhôm
Bài 19: Sắt
Bài 20: kim loại tổng hợp sắt: Gang, thép
Bài 21: Sự ăn uống mòn sắt kẽm kim loại và đảm bảo an toàn kim loại không biến thành ăn mòn
Bài 22: luyện tập chương 2: Kim loại
Bài 23: Thực hành: tính chất hóa học của nhôm cùng sắt
Bài 24: Ôn tập học tập kì 1
Xem toàn thể tài liệu Lớp 9: trên đây
Giải bài xích Tập hóa học 9 – bài xích 18: Nhôm giúp HS giải bài tập, cung ứng cho những em một khối hệ thống kiến thức và hiện ra thói quen học tập tập làm việc khoa học, làm căn nguyên cho câu hỏi phát triển năng lực nhận thức, năng lượng hành động:
Bài 1: Hãy điền vào bảng những đặc điểm tương ứng cùng với những áp dụng của nhôm:| Tính chất của nhôm | Ứng dụng của nhôm | |
| 1 | Làm dây dẫn điện | |
| 2 | Chế chế tạo ra máy bay, ô tô, xe cộ lửa, … | |
| 3 | Làm pháp luật gia đình: nỗi, xoong, … |
Lời giải:
| TÍNH CHẤT CỦA NHÔM | ỨNG DỤNG CỦA NHÔM | |
| 1 | Dẫn điện xuất sắc | có tác dụng dây dẫn năng lượng điện |
| 2 | Nhẹ, bền | chế tạo máy bay, ôtô, xe pháo lửa,… |
| 3 | Tính dẻo, dẫn sức nóng tốt, lạnh chảy ở lớn cao. | Làm luật pháp gia dụng: xoong, nồi, âm,… |
a) Mg
SO4.
Bạn đang xem: Giải bài tập hóa học 9
b) Cu
Cl2.
c) Ag
NO3.
d) HCl.
Cho biết hiện tượng lạ xảy ra? phân tích và lý giải và viết phương trình hóa học.
Lời giải:
a) không có phản ứng, vì hoạt động hóa học của Mg > Al.
b) Al chảy dần, blue color lam của dung dịch nhạt dần, bao gồm chất rắn màu đỏ bám vào mặt phẳng nhôm.
2Al + 3Cu
Cl2 → 2Al
Cl3 + 3Cu ↓
c) Al tung dần, có chất rắn color xám dính ngoài Al.
Al + 3Ag
NO3 → Al(NO3)3 + 3Ag ↓
d) có khí hiđro bay lên:
2Al + 6HCl → 2Al
Cl3 + 3H2 ↑ .
Lời giải:
Nếu sử dụng xô, chậu, nồi nhôm để đựng vôi, nước vôi hoặc vữa thì
Các điều khoản này có khả năng sẽ bị chóng hư vì trong vôi, nước vôi hoặc vữa đều sở hữu chứa Ca(OH)2 là 1 trong chất kiềm nên tính năng được với Al2O3 (vỏ bọc quanh đó các vật dụng bằng nhôm), tiếp nối đến Al bị ăn uống mòn.
Phương trình bội nghịch ứng:
Al2O3 + Ca(OH)2 → Ca(Al
O2)2 + H2O
2Al + Ca(OH)2 + 2H2O → Ca(Al
O2)2 + 3H2 ↑ .
Xem thêm: Giọng ải giọng ai
Bài 4: tất cả dung dịch muối AlCl3 lẫn tạp hóa học là Cu
Cl2. Rất có thể dùng chất nào sau đây để làm sạch muối bột nhôm? giải thích sự lựa chọn.
a) Ag
NO3.
b) HCl.
c) Mg.
d) Al.
e) Zn.
Lời giải:
d) sử dụng Al để gia công sạch muối hạt nhôm vì:
2Al + 3Cu
Cl2 → 2Al
Cl3 + 3Cu ↓
O2.2H2O. Hãy tính thành phần tỷ lệ theo cân nặng của Al gồm trogn hợp chất trên.
Lời giải:
M Al2O3.2Si
O2.2H2O = 27.2 + 16.3 + 2.(28 + 16.2) + 2.(2 + 16) = 258 (g)
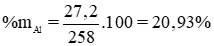
– phân tích 1: đến m gam tất cả hổn hợp A chức năng với hỗn hợp H2SO4 loãng dư, chiếm được 1568ml khí ở đk tiêu chuẩn.
– xem sét 2: cho m gam hỗn hợp A công dụng với hỗn hợp Na
OH dư thì sau phản nghịch ứng thấy còn lại 0,6g chất rắn.
Tính phần trăm trọng lượng của mỗi chất trong các thành phần hỗn hợp A.
Lời giải:
Ở thử nghiệm 2: Al tính năng hết cùng với Na
OH, còn Mg không phản ứng nên cân nặng chất rắn còn lại là Mg, m
Mg = 0,6g.








